> Περίληψη
Τα νεοπλάσματα του θυρεοειδή αδένα αφορούν το 1-3,8% του συνόλου των νεοπλασμάτων στον σκύλο και σε αυτά περιλαμβάνονται τα αδενώματα και τα καρκινώματα, με τα τελευταία να εμφανίζονται σε ποσοστό 90%. Η έκθεση σε ακτινοβολία, η ανεπάρκεια ιωδίου, ο υποθυρεοειδισμός και οι γενετικές μεταλλάξεις, αποτελούν μερικούς από τους αιτιολογικούς παράγοντες της εμφάνισής τους. Τα αδενώματα είναι μικρά και κινητά, χωρίς να διηθούν τους γύρω ιστούς και να έχουν μεταστάσεις. Αντιθέτως, τα καρκινώματα είναι μεγαλύτερου μεγέθους, παρουσιάζουν έντονα διηθητικό χαρακτήρα και τάση μετάστασης, συχνότερα στους πνεύμονες και στα επιχώρια λεμφογάγγλια. Η διάγνωση βασίζεται στη συμπτωματολογία που προκύπτει από την συμπίεση γειτονικών οργάνων (οισοφάγος, τραχεία, λάρυγγας, φάρυγγας), τον ορμονικό, και τον απεικονιστικό έλεγχο. Για την οριστική διάγνωση απαιτείται η πραγματοποίηση βιοψίας και ιστοπαθολογικής εξέτασης, η οποία επιβεβαιώνει την προέλευση της μάζας και διαφοροποιεί τα καλοήθη από τα κακοήθη νεοπλάσματα. Στα περιστατικά αδενώματος του θυρεοειδή, η χειρουργική εξαίρεση του νεοπλάσματος αποτελεί την θεραπεία εκλογής και οδηγεί στην ίαση του ζώου. Αναφορικά με το καρκίνωμα του θυρεοειδή, η επιλογή θεραπείας και η πρόγνωση εξαρτώνται από το μέγεθος του όγκου, τον βαθμό διήθησης των γειτονικών ιστών, την παρουσία μεταστάσεων και την δυνατότητα χρησιμοποίησης άλλων θεραπευτικών μέσων. Η χειρουργική θεραπεία ενδείκνυται στα περιστατικά μικρών και κινητών καρκινωμάτων ή με επιφανειακή διήθηση των γειτονικών ιστών, ενώ, αντενδείκνυται στις περιπτώσεις έντονα διηθητικών και μη κινητών καρκινωμάτων.
> Εισαγωγή
Τα νεοπλάσματα του θυρεοειδή αδένα αφορούν το 1-3,8 % του συνόλου των νεοπλασμάτων και το 10-15 % των νεοπλασμάτων που εμφανίζονται στις περιοχή της κεφαλής και του τραχήλου στο σκύλο, αντίστοιχα.1-5 Στα νεοπλάσματα του θυρεοειδή περιλαμβάνονται τα αδενώματα και τα καρκινώματα, που παρουσιάζονται συχνότερα, σε ποσοστό 90 % και εμφανίζονται σε ζώα ηλικίας 9-11 ετών.1,3,6-10 Οι φυλές Beagle, Siberian husky, Boxer και Golden retriever εμφανίζουν προδιάθεση στα νεοπλάσματα του θυρεοειδή,1,3,4,11,12 ενώ δεν έχει διαπιστωθεί προδιάθεση ως προς το φύλο.1-3,9-14
> Αιτιολογία και προδιαθετικοί παράγοντες
Έρευνες που έχουν πραγματοποιηθεί τόσο στον άνθρωπο όσο και στο σκύλο, απέδει- ξαν πως η έκθεση σε ακτινοβολία και η ανεπαρκής συγκέντρωση ιωδίου στον θυρεοειδή αδένα συνδέονται με την ανάπτυξη νεοπλασμάτων του.15 Η ανεπάρκεια ιωδίου, προκαλεί υπερέκκριση της θυρεοειδοτρόπου ορμόνης (TSH) από την υπόφυση, η οποία με την σειρά της οδηγεί σε υπερπλασία των επιθηλιακών κυττάρων του θυρεοειδή και πιθανόν στην νεοπλασματική εξαλλαγή τους.16,17 Ακόμη, έχει βρεθεί πως ο υποθυρεοειδισμός, που προκαλείται από λεμφοκυτταρική θυρεοειδίτιδα, συνδέεται με την νεοπλασματική εξαλλαγή του θυρεοειδή αδένα στο σκύλο.17 Έρευνες που πραγματοποιήθηκαν σε ανθρώπους, επιβεβαιώνουν πως διάφορες μεταλλάξεις στα ras ογκογονίδια και στα ογκοκατασταλτικά γονίδια, αποτελούν αιτίες νεοπλασματικής εξαλλαγής του θυρεοειδή και μετατροπής καλοήθων νεοπλάσματων σε κακοήθη, αντίστοιχα.18,19 Τέλος, η ανευπλοειδία αποτελεί κοινό χαρακτηριστικό του καρκινώματος του θυρεοειδή στο σκύλο και εμφανίζεται σε ποσοστό μεγαλύτερο από το 50% των περιστατικών με πρωτογενή νεοπλάσματα.20
> Βιολογική συμπεριφορά
Τα νεοπλάσματα του θυρεοειδή αδένα εμφανίζονται συχνότερα στην ανατομική περιοχή της εντόπισής του, δηλαδή στην κοιλιακή ή κοιλιακή και πλάγια επιφάνεια του τραχήλου, οπίσθια του λάρυγγα.3,10 O δεξιός και ο αριστερός λοβός προσβάλλονται στην ίδια συχνότητα, ενώ, αμφοτερόπλευρη προσβολή παρουσιάζεται στο 36-40% των περιστατικών με καρκίνωμα.1,7,8,11 Σπανιότερα παρατηρούνται νεοπλάσματα σε έκτοπες θέσεις όπως στην βάση της γλώσσας ή υπογλώσσια, στον υποδόριο ιστό ραχιαία της τραχείας,21 στο πρόσθιο μεσοπνευμόνιο, στην βάση της καρδιάς και σε άλλες ενδοκαρδιακές περιοχές.22-26 Τα αδενώματα αναπτύσσονται με αργό ρυθμό, είναι συνήθως μικρού μεγέθους, από μικροσκοπικά μέχρι διαμέτρου μερικών εκατοστών, μαλακά, συμπαγή, καλά εγκαψωμένα και εύκολα κινητά κατά τον προσθοπίσθιο άξονα κάτω από το δέρμα του τραχήλου. Αυτά δεν διηθούν τους γύρω ιστούς, δεν δίνουν μεταστάσεις και αποτελούν κυρίως τυχαίο εύρημα κατά την νεκροτομή.1,6,11
Τα καρκινώματα προέρχονται συχνότερα από τα κύτταρα των θυρεοειδών θυλακίων (αδενοκαρκίνωμα) και σπάνια από τα θυρεοπαραθυλακικά ή C κύτταρα (μυελοειδές καρκίνωμα).5,27,28 Αναπτύσσονται με γρήγορο ρυθμό και είναι συνήθως οζώδη, μεγαλύτερου μεγέθους από τα αδενώματα, από μικροσκοπικά μέχρι διαμέτρου μεγαλύτερης των 10 εκατοστών.1,3,29 Παρουσιάζουν έντονα διηθητικό χαρακτήρα προσβάλλοντας γειτονικές δομές όπως ο λάρυγγας, η τραχεία, οι σφαγίτιδες φλέβες και το καρωτιδικό έλυτρο και εμφανίζουν τάση για επιχώριες ή απομακρυσμένες μεταστάσεις.1,3,6 Τα καρκινώματα του θυρεοειδή, μεθίστανται κυρίως στους πνεύμονες και στα επιχώρια λεμφογάγγλια, ενώ, λιγότερο συχνά, δίνουν μεταστάσεις στη σφαγίτιδα φλέβα, στην καρδιά, στους νεφρούς, στα επινεφρίδια, στο ήπαρ, στο σπλήνα, στο έντερο, στο μεσεντέριο και στον εγκέφαλο.3,11 Οι πιθανότητες ύπαρξης μετάστασης κατά το χρόνο διάγνωσης κυμαίνονται από 16-38% και σχετίζονται άμεσα με το μέγεθος του νεοπλάσματος.3,6,7,10 Σε μία μεγάλη αναδρομική μελέτη παρατηρήθηκε ότι σκύλοι, στους οποίους ο όγκος του καρκινώματος ξεπερνούσε τα 100 cm3, παρουσίαζαν απομακρυσμένες μεταστάσεις σε ποσοστό 100%, ενώ στα καρκινώματα μεγέθους 21-100 cm3 και μικρότερου από 20 cm3 παρατηρήθηκε μετάσταση στο 74% και 14% των περιστατικών, αντίστοιχα.11
> Διάγνωση και Σταδιοποίηση
Κλινική εικόνα
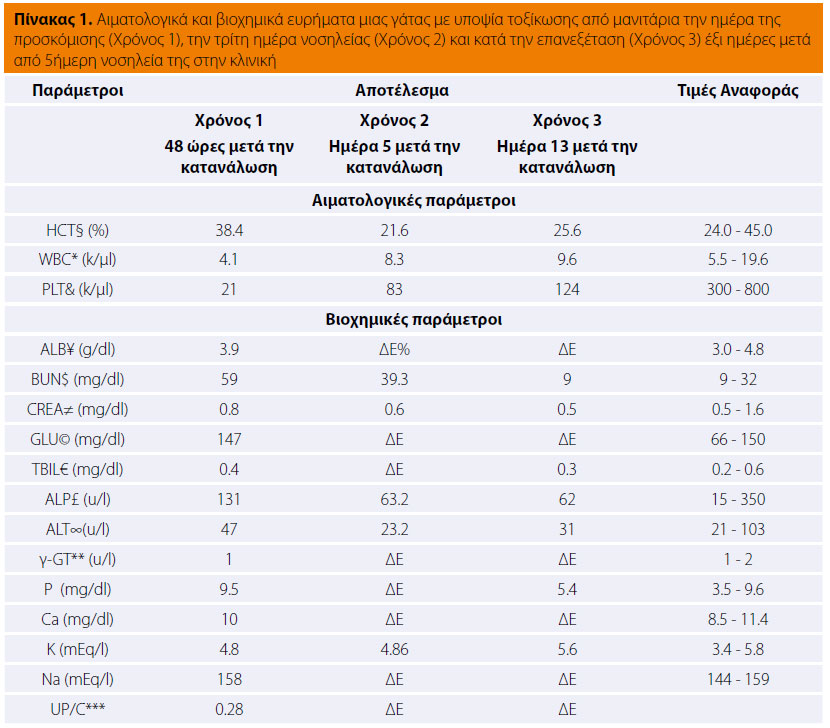
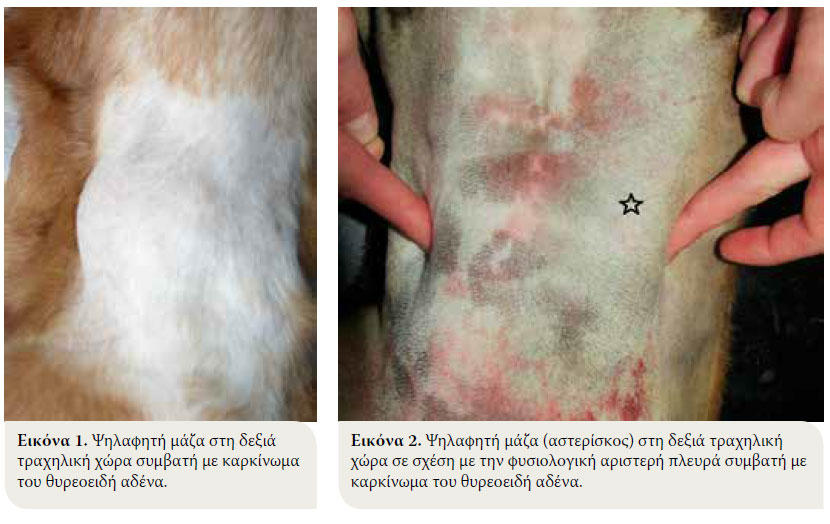
Η προσκόμιση του ζώου γίνεται συνήθως μετά από παρατήρηση από τον ιδιοκτήτη διόγκωσης στις περιοχές της κεφαλής και του τραχήλου, που σπανιότερα επεκτείνεται προς την είσοδο του θώρακα (Εικόνες 1, 2).1-3,7,10,11 Η διόγκωση αυτή βρίσκεται συνηθέστερα κοιλιακά της τραχείας (65-70 %), σχετίζεται με τον λάρυγγα και μπορεί να είναι καλά περιγεγραμμένη ή διεισδυτική.11 Οι πληροφορίες από το ιστορικό και την κλινική εξέταση μπορεί να αποκαλύψουν συμπτώματα από το αναπνευστικό και το πεπτικό σύστημα. Το αυξημένο μέγεθος του νεοπλάσματος, η μετάστασή του στους πνεύμονες και τα λεμφογάγγλια και η συμπίεση γειτονικών οργάνων (οισοφάγος, τραχεία, λάρυγγας, φάρυγγας), μπορεί να εκδηλωθούν με συμπτωματολογία που περιλαμβάνει αναπνευστική δυσχέρεια, βήχα, συριγμό, κυάνωση, πταρμό, ανάστροφο πταρμό, παράλυση του λάρυγγα, δυσφωνία, αναγωγή, έμετο, ληθαργικότητα, περιφερική λεμφαδενοπάθεια, πυρετό και σύνδρομο Horner.1-3,11,30
Σημειώνεται ότι κλινικά ευθυρεοειδικό παραμένει περίπου το 60% των σκύλων, ενώ περίπου το 30% εμφανίζει συμπτώματα υποθυρεοειδισμού, λόγω καταστροφής του φυσιολογικού παρεγχύματος του αδένα.1-3,11 Περιστατικά λειτουργικών νεοπλασμάτων έχουν αναφερθεί σε ποσοστό 10-22%, όπου τα ζώα παρουσίαζαν συμπτώματα υπερθυρεοειδισμού, παρόμοια με εκείνα των υπερθυρεοειδικών γατών, δηλαδή, πολυουρία, πολυδιψία, πολυφαγία με απώλεια βάρους, μυϊκή αδυναμία, νευρικότητα, εύκολη κόπωση, ταχυκαρδία και συνεχής αναζήτηση κρύων περιοχών στο σπίτι λόγω μη ανοχής στη ζέστη.3,29,31
Ορμονικός έλεγχος
Καθώς οι περισσότεροι σκύλοι εμφανίζονται κλινικώς ευθυρεοειδικοί, έχουν πραγματοποιηθεί μόνο λίγες κλινικές μελέτες που ελέγχουν την λειτουργία του θυρεοειδή μέσω μετρήσεων της συγκέντρωσης ορμονών όπως της τριιωδιοθυρονίνης (Τ3), της θυροξίνης (Τ4) και της TSH του πρόσθιου λοβού της υπόφυσης.3,11 Από μια έρευνα που πραγματοποιήθηκε σε 36 σκύλους με νεοπλάσματα του θυρεοειδή, το 39% παρουσίαζε μειωμένες τιμές Τ3 και Τ4, χωρίς όμως κανένας από αυτούς να παρουσιάζει συμπτώματα υποθυρεοειδισμού, ενώ, το 31% παρουσίαζε αυξημένες τιμές Τ4, με 2 μόνο να εμφανίζουν κλινικά συμπτώματα υπερθυρεοειδισμού.9 Ανεξάρτητα από την παρουσία ή όχι συμπτωμάτων υποθυρεοειδισμού ή υπερθυρεοειδισμού, προτείνεται να γίνεται σε όλα τα περιστατικά μέτρηση της ολικής Τ4, της ελεύθερης Τ4 και της TSH ώστε να αποσαφηνίζεται η λειτουργία του θυρεοειδή.32
Απεικονιστικές εξετάσεις
Ακτινολογικός έλεγχος
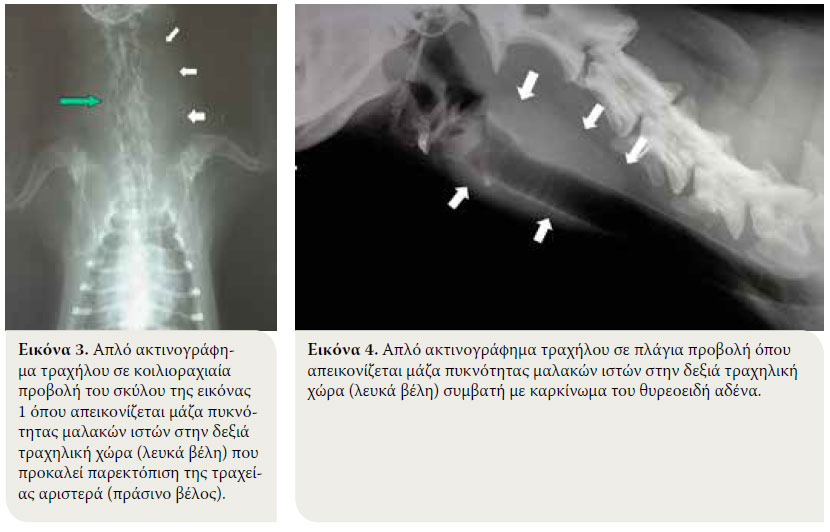
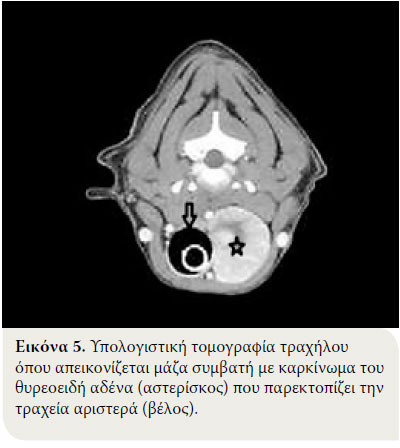
Η ακτινογράφηση της περιοχής του τραχήλου, σχεδόν πάντα, αποκαλύπτει την ύπαρξη μάζας πυκνότητας μαλακών ιστών που παρεκτοπίζει ή όχι την τραχεία ή τον λάρυγγα, αλλά δεν παρέχει πληροφορίες σχετικά με την αγγείωση και την διήθηση των γύρω ιστών (Εικόνες 3, 4).6 Η ακτινογράφηση του θώρακα, αποκαλύπτει την ύπαρξη πνευμονικών μεταστάσεων μόνο σε ποσοστό 33-77%.1-3,11 Στην περίπτωση που διαπιστωθούν ευρήματα από το μεσοπνευμόνιο συμβατά με μάζα πυκνότητας μαλακών ιστών που μπορεί να σχετίζεται με έκτοπο νεόπλασμα του θυρεοειδή αδένα, προτείνεται ο υπερηχοτομογραφικός έλεγχος του θώρακα επειδή η ύπαρξη υγρού ή λίπους στην υπεζωκοτική κοιλότητα ή στο μεσοπνευμόνιο χώρο μπορεί να μοιάζει με μάζα στην απλή ακτινογραφία.30,33
Υπερηχοτομογραφική εξέταση
Πρόκειται για μια πολύτιμη, σχετικά φθηνή, μη επεμβατική μέθοδο απεικόνισης, στην οποία σπάνια απαιτείται η αναισθησία του ζώου. Για τους λόγους αυτούς, πολλές φορές χρησιμοποιείται ως μέθοδος εκλογής για την εξέταση της μορφολογίας του θυρεοειδή αδένα. Ο υπερηχοτομογραφικός έλεγχος μπορεί να διακρίνει μάζες >2mm και να διαχωρίζει τα συμπαγή από τα κυστικά οζίδια. Συνεπώς, αλλοιώσεις <2 cm προτείνεται να αξιολογούνται υπερηχοτομογραφικά.34 Οι πληροφορίες που παρέχει βοηθούν στην διαφοροποίηση των νεοπλάσματων του θυρεοειδή από άλλες μάζες που μπορεί να υπάρχουν στην κοιλιακή περιοχή του τραχήλου και στη διάκριση ετερόπλευρης ή αμφοτερόπλευρης προσβολής του αδένα.35 Ωστόσο, μερικές φορές είναι δύσκολο να τεκμηριωθεί η θυρεοειδική προέλευση της μάζας, εάν η φυσιολογική ανατομία της τραχηλικής χώρας έχει αλλοιωθεί.33,36 Επιπλέον, παρέχει πληροφορίες για τον βαθμό αγγείωσης του νεοπλάσματος και της διήθησης των γύρω ιστών, χωρίς όμως να διαφοροποιεί τα καλοήθη από τα κακοήθη νεοπλάσματα, εκτός και αν διαπιστωθεί περιφερική λεμφαδενοπάθεια και τοπική διήθηση.33 Σε περίπτωση νεοπλάσματος με εκτεταμένη αγγείωση συνιστάται βιοψία με υπερηχοτομογραφική καθοδήγηση ώστε να αποφευχθεί πρόκληση αιμορραγίας.30,33
 Υπολογιστική τομογραφία (CT) και απεικόνιση μαγνητικού συντονισμού (MRI)
Υπολογιστική τομογραφία (CT) και απεικόνιση μαγνητικού συντονισμού (MRI)
Οι τεχνικές αυτές ενδείκνυνται για μάζες >3cm και παρέχουν χρήσιμες πληροφορίες σε ότι αφορά την προέλευση και τον βαθμό αγγείωσης τους, καθώς επίσης και τον βαθμό διήθησης των γύρω ιστών.30,34 Επιπλέον, προσφέρουν την δυνατότητα διερεύνησης του θώρακα για την ανίχνευση μεταστάσεων στους πνεύμονες και παρουσίας έκτοπου ενδοθωρακικού θυρεοειδικού ιστού, ενώ ακόμα μπορούν να εντοπίσουν μεταστάσεις στα λεμφογάγγλια.34 Τέλος, η CT επιτρέπει τη σταδιοποίηση του καρκινώματος του θυρεοειδή.37
Συμπερασματικά, και οι 3 απεικονιστικές τεχνικές (υπερηχοτομογραφία, CT ή MRI) δίνουν σχεδόν τις ίδιες πληροφορίες για τα χαρακτηριστικά που πρέπει να αναζητούνται όταν διαπιστώνεται η παρουσία μάζας στην τραχηλική χώρα. Σε μια έρευνα που συνέκρινε την ευαισθησία και την ειδικότητα αυτών των τεχνικών σε 13 περιστατικά σκύλων με καρκίνωμα του θυρεοειδή βρέθηκε ότι η υπερηχοτομογραφία είχε ευαισθησία 79% και ειδικότητα 33%, η CT 85% και 100% αντίστοιχα και ο MRI 93% και 67% αντίστοιχα.36 Στις περιπτώσεις που η ερμηνεία των αποτελεσμάτων που προκύπτουν από τις απεικονιστικές εξετάσεις είναι αμφιλεγόμενη, η χειρουργική διερεύνηση της τραχηλικής χώρας, αποτελεί έναν γρήγορο, ακριβή και φθηνό τρόπο, με τον οποίο διαπιστώνεται η διεισδυτικότητα και η προέλευση της μάζας.38
Κυτταρολογική εξέταση
Η παρακέντηση της μάζας με την βοήθεια λεπτής βελόνας (FNA) αποτελεί μια μη επεμβατική, γρήγορη και εύκολη μέθοδο, για την οποία δεν χρειάζεται να προηγηθούν ηρέμηση ή γενική αναισθησία.38 Έρευνες έχουν δείξει πως η κυτταρολογική εξέταση μετά από FNA ταυτοποιεί την θυρεοειδική προέλευση μάζας που βρίσκεται στην τραχηλική χώρα, σε περισσότερα από τα μισά περιστατικά σκύλων με νεόπλασμα του θυρεοειδή, χωρίς όμως να διαφοροποιεί τα καλοήθη από τα κακοήθη νεοπλάσματα.3,29 Η επιμόλυνση των δειγμάτων με αίμα λόγω της μεγάλης αγγείωσης της μάζας, η ευθραυστότητα των κυττάρων των θυρεοειδικών θυλακίων και η ενεργή φλεγμονή τους, αποτελούν μερικούς από τους λόγους που περιορίζουν την διαγνωστική ακρίβεια της μεθόδου αυτής.29 Για την ελαχιστοποίηση της επιμόλυνσης των δειγμάτων με αίμα, συστήνεται η παρακέντηση να γίνεται με υπερηχοτομογραφική καθοδήγηση.30,33
Βιοψία και ιστοπαθολογική εξέταση
Σε μικρές (<7cm) ή/και κινητές μάζες, η βιοψία με χειρουργική εκτομή βρίσκει τόσο διαγνωστική όσο και θεραπευτική εφαρμογή. Η βιοψία από μεγάλες και έντονα διηθητικές μάζες γίνεται με βελόνα τύπου Tru-cut ή με τομή με τον κίνδυνο όμως εμφάνισης σοβαρών αιμορραγιών.6,39 Για τον λόγο αυτό, προτείνεται η ανοιχτή βιοψία ώστε αυτή να πραγματοποιείται στο σημείο με την λιγότερη αγγείωση, ενώ επιπλέον υπάρχει η δυνατότητα επίσχεσης της αιμορραγίας εφόσον κριθεί απαραίτητη.39
Για την οριστική διάγνωση των θυρεοειδικών νεοπλασμάτων απαιτείται βιοψία και ιστοπαθολογική εξέταση, η οποία όχι μόνο επιβεβαιώνει την προέλευση της μάζας, αλλά διαφοροποιεί και τα καλοήθη από τα κακοήθη νεοπλάσματα.29 Με βάση την ιστολογική εικόνα, τα νεοπλάσματα του θυρεοειδή, προέρχονται είτε από τα κύτταρα των θυρεοειδών θυλακίων, είτε από τα θυρεοπαραθυλακικά ή C-κύτταρα.
Η κακοήθεια στα καλά διαφοροποιημένα νεοπλάσματα, χαρακτηρίζεται από διήθηση της κάψας και αγγειακή διήθηση.40 Τα περισσότερα καρκινώματα του θυρεοειδή στον σκύλο είναι καλά προς μέτρια διαφοροποιημένα και προέρχονται συνήθως από τα κύτταρα των θυρεοειδών θυλακίων. Η συμπαγής-θυλακιώδης μορφή απαντάται σε μεγαλύτερη συχνότητα, ενώ ακολουθούν οι μορφές θυλακιώδης και συμπαγής.3,7,24 Τα αδενώματα των κυττάρων των θυρεοειδών θυλακίων εμφανίζονται συνηθέστερα με την θυλακιώδη μορφή.11,41 Η θηλώδης μορφή του καρκινώματος των κυττάρων των θυρεοειδών θυλακίων, το μυελοειδές καρκίνωμα (θυρεοπαραθυλακικά ή C-κύτταρα) και τα μη διαφοροποιημένα καρκινώματα, εμφανίζονται σπάνια στον σκύλο.1-3,11,28 Ο χρόνος επιβίωσης των σκύλων με καρκίνωμα του θυρεοειδή, δεν φαίνεται να σχετίζεται σημαντικά με την ιστοπαθολογική σταδιοποίησή του.3,7
Σταδιοποίηση
Η κλινική σταδιοποίηση γίνεται σύμφωνα με τον Παγκόσμιο Οργανισμό Υγείας [WHO Tumor Node Metastasis (TNM) Staging System] και παρουσιάζεται στον Πίνακα 1. Με το σύστημα αυτό, το νεόπλασμα κατηγοριοποιείται ανάλογα με το μέγεθος και την διεισδυτικότητα του στους γειτονικούς ιστούς (Τ), την μετάσταση στα επιχώρια λεμφογάγγλια (N) ή την παρουσία απομακρυσμένης μετάστασης (Μ).42

> Διαφορική διάγνωση
Τα νεοπλάσματα του θυρεοειδή θα πρέπει να διαφοροποιηθούν από τα αποστήματα, τα κοκκιώματα, τις σιελογόνες βλεννοκήλες, τη λεμφογενή μετάσταση του καρκινώματος του πλακώδους επιθηλίου των αμυγδαλών, το λέμφωμα, το νεόπλασμα του καρωτιδικού σώματος και τα σαρκώματα.43
> Θεραπεία
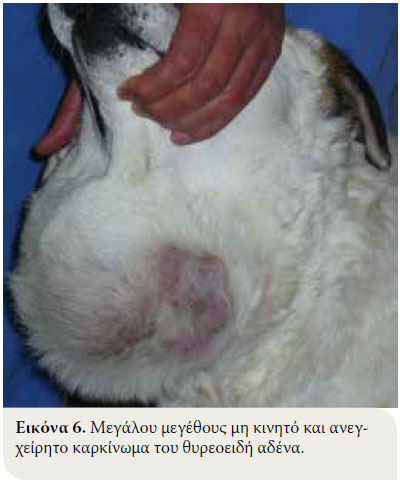 Στα περιστατικά αδενώματος του θυρεοειδή, η χειρουργική εξαίρεση του νεοπλάσματος αποτελεί την θεραπεία εκλογής και οδηγεί στην ίαση του ζώου.6,32 Αναφορικά με το καρκίνωμα του θυρεοειδή η επιλογή θεραπείας εξαρτάται από παράγοντες όπως το μέγεθος του όγκου, το βαθμό διήθησης των γειτονικών ιστών, την παρουσία μεταστάσεων και τη δυνατότητα χρησιμοποίησης άλλων θεραπευτικών μέσων (ακτινοθεραπεία, χημειοθεραπεία).43 Γενικά, η χειρουργική θεραπεία ενδείκνυται στα περιστατικά μικρών (<7cm) και κινητών νεοπλασμάτων ή σε νεοπλάσματα με επιφανειακή διήθηση των γειτονικών ιστών, ενώ, αντενδείκνυται στις περιπτώσεις έντονα διηθητικών και μη κινητών νεοπλασμάτων (Εικόνα6).6,7,10,32 Πολλές φορές είναι απαραίτητη η χειρουργική διερεύνηση του καρκινώματος για να διαπιστωθεί ο βαθμός διήθησης των γειτονικών ιστών. Στα περιστατικά που διαγιγνώσκονται με μεταστατική νόσο, η θεραπεία που αναλαμβάνεται είναι παρηγορητική και περιλαμβάνει την ακτινοθεραπεία ή τη χορήγηση ραδιενεργού ιωδίου ή το συνδυασμό χειρουργική εξαίρεσης και ακτινοθεραπείας. Όταν μετά τον απεικονιστικό έλεγχο δεν διαπιστωθούν μεταστάσεις, η επιλογή της θεραπείας θα βασιστεί στο κατά πόσο το νεόπλασμα είναι κινητό ή όχι. Εφόσον είναι κινητό, επιλέγεται η χειρουργική εξαίρεση του, πραγματοποιώντας ετερόπλευρη ή σπάνια αμφοτερόπλευρη θυρεοειδεκτομή, συνδυαστικά ή όχι με ακτινοθεραπεία. Εφόσον το νεόπλασμα είναι μη κινητό, η χειρουργική θεραπεία αντενδείκνυται και προτείνονται ακτινοθεραπεία και θεραπεία με ραδιενεργό ιώδιο.32
Στα περιστατικά αδενώματος του θυρεοειδή, η χειρουργική εξαίρεση του νεοπλάσματος αποτελεί την θεραπεία εκλογής και οδηγεί στην ίαση του ζώου.6,32 Αναφορικά με το καρκίνωμα του θυρεοειδή η επιλογή θεραπείας εξαρτάται από παράγοντες όπως το μέγεθος του όγκου, το βαθμό διήθησης των γειτονικών ιστών, την παρουσία μεταστάσεων και τη δυνατότητα χρησιμοποίησης άλλων θεραπευτικών μέσων (ακτινοθεραπεία, χημειοθεραπεία).43 Γενικά, η χειρουργική θεραπεία ενδείκνυται στα περιστατικά μικρών (<7cm) και κινητών νεοπλασμάτων ή σε νεοπλάσματα με επιφανειακή διήθηση των γειτονικών ιστών, ενώ, αντενδείκνυται στις περιπτώσεις έντονα διηθητικών και μη κινητών νεοπλασμάτων (Εικόνα6).6,7,10,32 Πολλές φορές είναι απαραίτητη η χειρουργική διερεύνηση του καρκινώματος για να διαπιστωθεί ο βαθμός διήθησης των γειτονικών ιστών. Στα περιστατικά που διαγιγνώσκονται με μεταστατική νόσο, η θεραπεία που αναλαμβάνεται είναι παρηγορητική και περιλαμβάνει την ακτινοθεραπεία ή τη χορήγηση ραδιενεργού ιωδίου ή το συνδυασμό χειρουργική εξαίρεσης και ακτινοθεραπείας. Όταν μετά τον απεικονιστικό έλεγχο δεν διαπιστωθούν μεταστάσεις, η επιλογή της θεραπείας θα βασιστεί στο κατά πόσο το νεόπλασμα είναι κινητό ή όχι. Εφόσον είναι κινητό, επιλέγεται η χειρουργική εξαίρεση του, πραγματοποιώντας ετερόπλευρη ή σπάνια αμφοτερόπλευρη θυρεοειδεκτομή, συνδυαστικά ή όχι με ακτινοθεραπεία. Εφόσον το νεόπλασμα είναι μη κινητό, η χειρουργική θεραπεία αντενδείκνυται και προτείνονται ακτινοθεραπεία και θεραπεία με ραδιενεργό ιώδιο.32
Χειρουργική θεραπεία
Χειρουργική ανατομική
Η καλή γνώση της ανατομικής του τραχήλου και ειδικότερα του θυρεοειδή είναι απαραίτητη για την απρόσκοπτη και ασφαλή χειρουργική διερεύνηση και αντιμετώπιση των νεοπλασμάτων του θυρεοειδή. Ο θυρεοειδής αδένας, αποτελείται από δύο επιμήκεις λοβούς και εντοπίζεται στην αρχή της τραχηλικής μοίρας της τραχείας. Συνήθως, ο δεξιός λοβός βρίσκεται στο ύψος των 5 πρώτων τραχειακών ημικρικίων, ενώ ο αριστερός λοβός εντοπίζεται οπισθιότερα, εκτεινόμενος από το 3ο μέχρι το 8ο τραχειακό ημικρίκιο. Οι λοβοί εφάπτονται κοιλιακά με τους στερνοϋοειδή και στερνοκεφαλικό μυ, ενώ στα πλάγια με τον στερνοθυρεοειδή μυ. Οι λοβοί βρίσκονται σε κοντινή απόσταση από την καρωτίδα, τον πλανητικοσυμπαθητικό κλώνο και την σφαγίτιδα φλέβα (Εικόνα 7).44-45
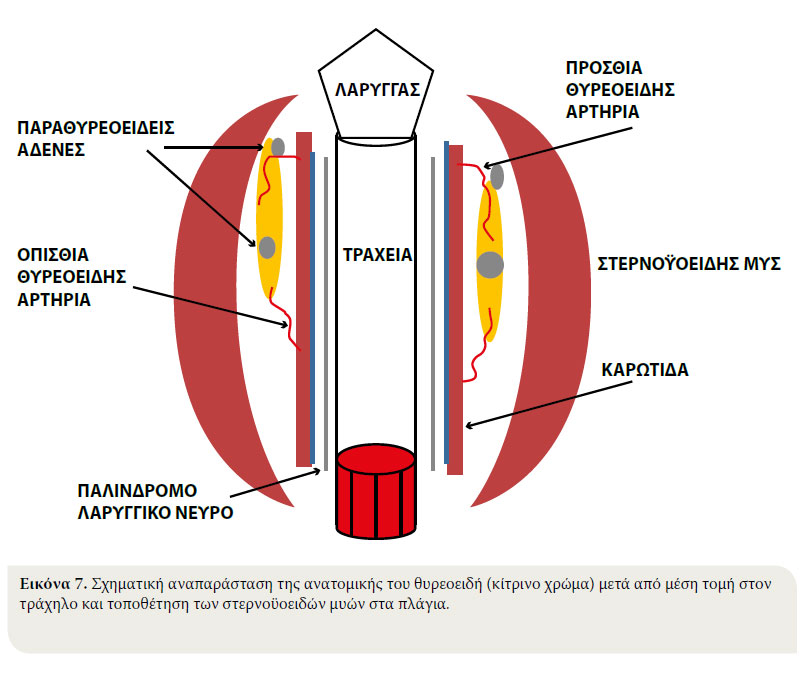
Οι παραθυρεοειδείς αδένες συνδέονται στενά με τον θυρεοειδή αδένα και είναι συνήθως δύο για κάθε λοβό του θυρεοειδή: ένας έξω, που βρίσκεται στο πρόσθιο άκρο του λοβού και ένας έσω, που εντοπίζεται στην εσωτερική επιφάνεια του λοβού, κάτω από την ινώδη κάψα του ή μέσα στο παρέγχυμά του.44-45
Η αιμάτωση του θυρεοειδή αδένα πραγματοποιείται από την πρόσθια και οπίσθια θυρεοειδή αρτηρία. Η πρόσθια θυρεοειδής αρτηρία εκφύεται από την καρωτίδα και η οπίσθια θυρεοειδής αρτηρία εκφύεται από την βραχιονοκεφαλική αρτηρία. Η φλεβική αποχέτευση του αίματος γίνεται μέσω της πρόσθιας θυρεοειδούς φλέβας, η οποία αποχετεύει το περιεχόμενό της στη σφαγίτιδα.44-45
Προεγχειρητική προετοιμασία
Εφόσον έχει επιλεχθεί η χειρουργική εξαίρεση του νεοπλάσματος, όπως και σε κάθε άλλη χειρουργική επέμβαση, πρέπει να εκτιμηθεί η κατάσταση της υγείας του ασθενούς με την πραγματοποίηση των κατάλληλων αιματολογικών και βιοχημικών εξετάσεων. Επιπλέον, λόγω της εκτεταμένης αγγείωσης του θυρεοειδή και μερικές φορές της διήθησης μεγάλων αγγείων, κατά τη θυρεοειδεκτομή, αναμένονται μεγάλες αιμορραγίες και μερικές φορές σοβαρή απώλεια αίματος. Το γεγονός αυτό καθιστά απαραίτητο τον έλεγχο του αιμοστατικού μηχανισμού και την προετοιμασία για πιθανή μετάγγιση διεγχειρητικά ή μετεγχειρητικά.32,43,46 Η αναισθησία πραγματοποιείται κατά τα γνωστά αφού σπάνια το νεόπλασμα του θυρεοειδή είναι λειτουργικό.43 Σημειώνεται ότι ακόμα και στις περιπτώσεις υπερθυρεοειδικών ζώων, η προσπάθεια μετάβασης τους σε ευθυρεοειδική κατάσταση πριν την χειρουργική επέμβαση δεν είναι απαραίτητη, σε αντίθεση με ότι συμβαίνει στις υπερθυρεοειδικές γάτες. Σε οποιαδήποτε όμως περίπτωση παρατηρηθούν σοβαρές περιεγχειρητικές αρρυθμίες ή σοβαρή υπέρταση, χορηγείται η κατάλληλη αγωγή.31
Θυρεοειδεκτομή 32,38,39,47
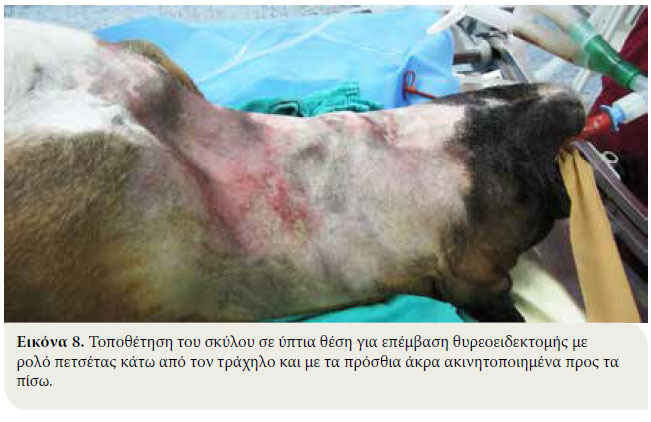
- Μετά την εγκατάσταση της αναισθησίας, το ζώο τοποθετείται σε ύπτια θέση, τα πρόσθια άκρα δένονται προς τα πίσω, κάτω από τον τράχηλο τοποθετείται μια αναδιπλωμένη πετσέτα, έτσι ώστε αυτός να βρίσκεται σε ήπια υπερέκταση και επιπλέον στον οισοφάγο τοποθετείται σωλήνας που διευκολύνει την ανεύρεσή του κατά την διάρκεια της χειρουργικής επέμβασης. Η κοιλιακή επιφάνεια του τραχήλου, από το πίσω μέρος της κάτω γνάθου μέχρι την λαβή του στέρνου, προετοιμάζεται χειρουργικά (Εικόνα 8).
- Πραγματοποιείται μέση τραχηλική τομή, που εκτείνεται από το θυρεοειδή χόνδρο του λάρυγγα μέχρι την λαβή του στέρνου.
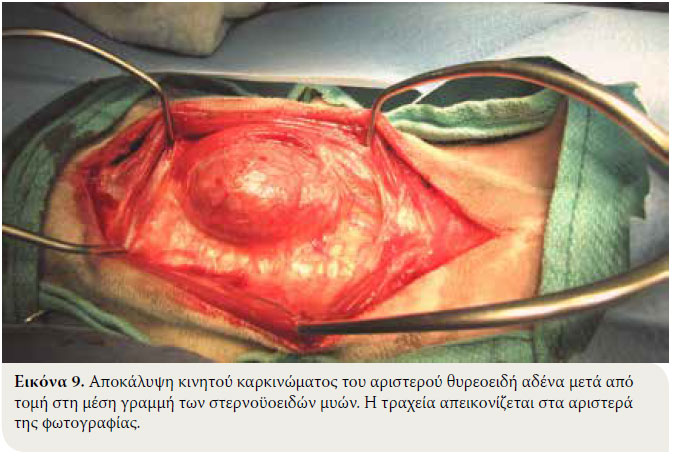
- Με την βοήθεια μαχαιριδίου γίνεται διατομή των εγκάρσιων μυών του επιπολής σφιγκτήρα του τραχήλου, έτσι ώστε να αποκαλυφθεί το ζεύγος των στερνοϋοειδών μυών. Γίνεται τομή στη μέση γραμμή των μυών αφού γίνει αιμόσταση των μικρών αγγείων που πορεύονται στη ραφή των μυών με διαθερμία ή απολίνωση. Η τραχεία αποκαλύπτεται, ενώ ταυτόχρονα εμφανίζονται οι λοβοί του θυρεοειδή αδένα που βρίσκονται ραχιαία ή ραχιαία και πλάγια της τραχείας, κοντά στον θυρεοειδή χόνδρο (Εικόνα 9).
- Αν ο θυρεοειδής αδένας δεν είναι ορατός, γίνεται απώθηση από την μέση γραμμή του ζεύγους των στερνοθυρεοειδών μυών, οι οποίοι βρίσκονται ραχιαία και προς τα έσω των στερνοϋοειδών μυών. Για την ευχερέστερη επισκόπηση του πεδίου συνιστάται η απαγωγή των στενοϋοειδών και στερνοθυρεοειδών μυών με την τοποθέτηση 2 διαστολέων Gelpi στο πρόσθιο και οπίσθιο τμήμα της τομής.
- Επισκοπούνται προσεχτικά και οι δύο λοβοί του θυρεοειδή, καθώς επίσης και η σχέση τους με τις γύρω ανατομικές δομές.
- Αποκαλύπτονται τα παλίνδρομα λαρυγγικά νεύρα, τα οποία πορεύονται κατά μήκος της τραχείας και προς τα έσω του αδένα ή στην περιτονία ραχιαία του αδένα. Κατά την φάση της θυρεοειδεκτομής, λαμβάνεται μέριμνα, ώστε να αποφευχθεί κάκωση των νεύρων αυτών.
- Γίνεται απολίνωση των αγγείων που περιβάλουν τον αδένα. Η οπίσθια θυρεοειδής αρτηρία απολινώνεται και αφού γίνει διατομή των ιστών ραχιαία του αδένα, αυτός διατέμνεται και φέρεται προς τα εμπρός για να γίνει η απολίνωση της πρόσθιας θυρεοειδούς αρτηρίας. Οι απολινώσεις γίνονται με συνθετικό απορροφήσιμο ράμμα 3/0 ή με αγγειακά clips (Εικόνες 10, 11). Στις περιπτώσεις που παρατηρούνται μεγάλες αιμορραγίες εξαιτίας της εκτεταμένης νεοαγγείωσης, κρίνεται σκόπιμη η προσωρινή ετερόπλευρη απολίνωση της καρωτίδας και της σφαγίτιδας φλέβας, η οποία είναι καλά ανεκτή από το ζώο.
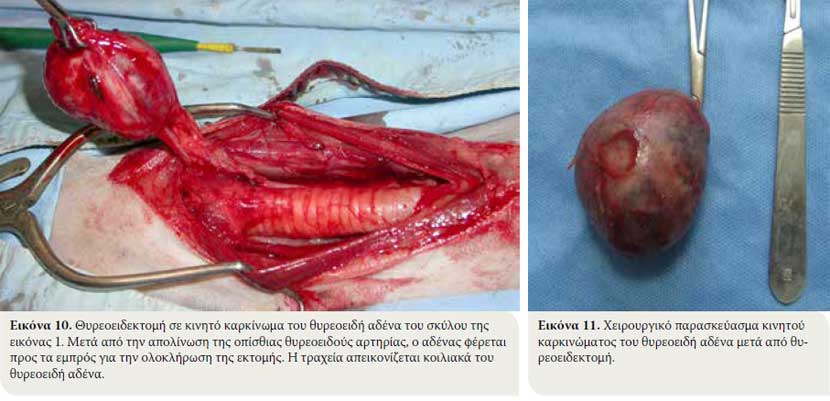
- Στην περίπτωση έντονα διηθητικού καρκινώματος που εισβάλλει τους γύρω ιστούς και δομές, όπως, τη σύστοιχη σφαγίτιδα φλέβα, την καρωτίδα, τον πλανητικοσυμπαθητικό κλώνο και το παλίνδρομο λαρυγγικό νεύρο, αυτά εκτέμνονται και αφαιρούνται ετερόπλευρα en block, χωρίς πρόβλημα παρά μόνο την εμφάνιση ετερόπλευρου συνδρόμου Horner. Αντίθετα, όταν το καρκίνωμα φαίνεται να διηθεί την τραχεία ή/και τον οισοφάγο ή υπάρχει εκτεταμένη νεοαγγείωση, τότε το νεόπλασμα θεωρείται ανεγχείρητο.
- Η αμφοτερόπλευρη προσβολή των αδένων, εφόσον είναι κινητοί, μπορεί να αντιμετωπιστεί με αμφοτερόπλευρη θυρεοειδεκτομή με διατήρηση ή όχι των παραθυρεοειδών αδένων. Σε περίπτωση όμως ολικής παραθυρεοειδεκτομής απαιτείται αντιμετώπιση της διαταραχής της ομοιοστασίας του ασβεστίου.
- Η σύγκλειση των μυών στη μέση γραμμή γίνεται με απορροφήσιμο ράμμα 3/0 και η σύγκλιση του υποδόριου ιστού και του δέρματος πραγματοποιείται κατά τα γνωστά.
Μετεγχειρητική παρακολούθηση και επιπλοκές
Η μετεγχειρητική αιμορραγία σε ζώα που υποβλήθηκαν σε θυρεοειδεκτομή μπορεί να είναι σοβαρή. Όταν οι αιμορραγίες είναι μικρές τότε αρκεί η εφαρμογή ψυχρών επιθεμάτων στην περιοχή και η επίδεση του τραχήλου. Σε σοβαρές αιμορραγίες είναι απαραίτητη η μετάγγιση αίματος ή/και η επαναδιερεύνηση του τραύματος με σκοπό την επίσχεση της αιμορραγίας.32,43,46
Κατά τη θυρεοειδεκτομή -εφόσον δεν έχει αναγνωριστεί και προστατευτεί κατάλληλα- το παλίνδρομο λαρυγγικό νεύρο μπορεί να υποστεί κάκωση. Κατά την αφαίρεση μεγάλων όγκων μπορεί να επέλθει νευραπραξία λόγω έλξης και διάτασης του νεύρου ή να χρειαστεί εκτομή του νεύρου εφόσον διηθείται από τον όγκο. Στις περιπτώσεις αυτές και εφόσον η βλάβη είναι ετερόπλευρη συνήθως δεν έχει επιπτώσεις στην αναπνευστική λειτουργία. Επιπλέον, μπορεί να παρατηρηθεί διαταραχή της φωνής (αλλαγή της χροιάς, δυσφωνία, αφωνία).46 Παράλυση του λάρυγγα παρατηρείται συνήθως μετά από αμφοτερόπλευρο τραυματισμό των παλίνδρομων λαρυγγικών νεύρων σε αμφοτερόπλευρη θυρεοειδεκτομή, Στις περιπτώσεις αυτές συνιστάται κρικοαρυταινοειδική λαρυγγοπλαστική.46 Στην περίπτωση κάκωσης του πνευμονογαστρικού νεύρου μπορεί να εμφανιστεί ετερόπλευρο σύνδρομο Horner, ενώ σε αμφοτερόπλευρο τραυματισμό ή/και διατομή του πνευμονογαστρικού νεύρου, αναμένεται η εμφάνιση μεγαοισοφάγου.32,43
Μετά από αμφοτερόπλευρη ολική θυρεοειδεκτομή και συναφαίρεση των παραθυρεοειδών αδένων η πλεινότητα των περιστατικών αναπτύσσει μόνιμο υποπαραθυρεοειδισμό και ως συνέπεια αυτού υπασβεστιαιμία.32 Εάν εμφανιστούν συμπτώματα υπασβεστιαιμίας (νευρικότητα, μυϊκός τρόμος, επιληπτικές κρίσεις) χορηγείται ενδοφλεβίως και με αργό ρυθμό γλυκονικό ασβέστιο 10%. Στα ζώα με υποθυρεοειδισμό και υπασβεστιαιμία χορηγούνται δια βίου βιταμίνη D και συμπληρώματα ασβεστίου με την πρώτη χορήγηση βιταμίνης D να γίνεται 12 ώρες μετά την επέμβαση.48
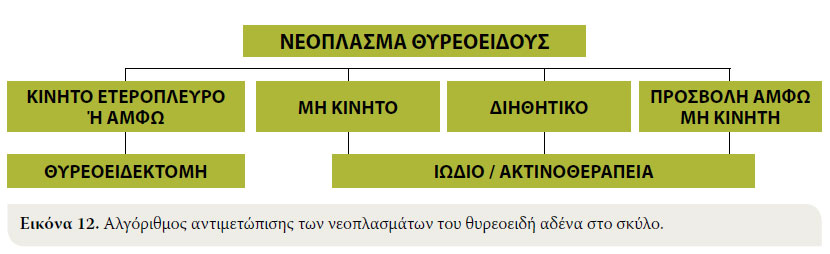
Επιπλέον, μετά από αμφοτερόπλευρη θυρεοειδεκτομή υπάρχει πιθανότητα εμφάνισης υποθυρεοειδισμού, για αυτό και πρέπει σε τακτά χρονικά διαστήματα να ελέγχονται εργαστηριακά οι συγκεντρώσεις των ορμονών του θυρεοειδή. Στις περιπτώσεις αυτές χορηγούνται ορμονικά σκευάσματα όπως η νατριούχος L-θυροξίνη ή λεβοθυροξίνη.46 Ο αλγόριθμος αντιμετώπισης των νεοπλασμάτων του θυρεοειδή αδένα παρατίθεται στην Εικόνα 12.
Πρόγνωση
Στα περιστατικά αδενώματος του θυρεοειδή η πρόγνωση είναι πολύ καλή, καθώς η πλήρης χειρουργική εξαίρεση του νεοπλάσματος οδηγεί στην ίαση του ζώου.
Η πρόγνωση στα περιστατικά με καρκίνωμα του θυρεοειδή αδένα σχετίζεται με το μέγεθος και την διεισδυτικότητα του νεοπλάσματος, καθώς επίσης και την ύπαρξη μεταστάσεων, ενώ δεν φαίνεται να υπάρχει συσχέτιση μεταξύ της αγγειακής πυκνότητάς τους και του χρόνου επιβίωσης.40 Σε δύο μελέτες που πραγματοποιήθηκαν σε σκύλους με κινητά, μη διηθητικά καρκινώματα που είχαν υποβληθεί σε χειρουργική αφαίρεση, αυτοί παρουσίασαν μέσο χρόνο επιβίωσης 1-3 χρόνια στην μία, ενώ αντιθέτως, στην άλλη μόνο 7 μήνες.3,40 Επίσης, μία άλλη μεγάλη έρευνα σε 82 σκύλους με καρκίνωμα του θυρεοειδή, αποκάλυψε πως οι 20 οι οποίοι είχαν κινητό καρκίνωμα, χωρίς ενδείξεις μετάστασης, όταν υποβλήθηκαν σε χειρουργική αφαίρεση, ο μέσος χρόνος επιβίωσης τους ήταν 36 μήνες.7 Σε σκύλους με ανεγχείρητο καρκίνωμα, στους οποίους δεν πραγματοποιήθηκε καμία άλλη θεραπεία, μία κλινική μελέτη έδειξε πως από τους 8, οι 5 έζησαν για περίπου 6 μήνες και οι 2 για τουλάχιστον 1 χρόνο, ενώ σε μία άλλη έρευνα ο μέσος χρόνος επιβίωσης ήταν οι 3 μήνες.9,10 Πρόσφατα σε μελέτη 15 σκύλων με κινητό αμφοτερόπλευρο καρκίνωμα του θυρεοειδή που υποβλήθηκαν σε αμφοτερόπλευρη θυρεοειδεκτομή με ή χωρίς συναφαίρεση των παραθυρεοειδών βρέθηκε ότι ο μέσος χρόνος επιβίωσης ήταν 38,3 μήνες. 11 ζώα εμφάνισαν υπασβεστιαιμία κατά την άμεση μετεγχειρητική περίοδο, και στο τέλος της μελέτης 7 λάμβαναν θεραπεία για αυτή, ενώ σε 8 γίνονταν αντιμετώπιση του υποθυρεοειδισμού.49 Τέλος, σε ότι αφορά την πρόγνωση σε σκύλους με μυελοειδές καρκίνωμα, δεν είναι γνωστό αν αυτή είναι ευνοϊκότερη σε σχέση με αυτή του καρκίνωματος. Σημειώνεται ότι το μυελοειδές καρκίνωμα είναι καλύτερα εγκαψωμένο και έχει μικρότερη τάση διήθησης των γύρω ιστών συγκριτικά με το αδενοκαρκίνωμα.10
Ακτινοθεραπεία
Η ακτινοθεραπεία μπορεί να φανεί αρκετά αποτελεσματική σε περιπτώσεις έντονα διηθητικών και ανεγχείρητων νεοπλασμάτων και πραγματοποιείται είτε ως μονοθεραπεία, είτε σε συνδυασμό με τη χειρουργική θεραπεία, η οποία γίνεται σε δεύτερο χρόνο, αφού επέλθει μείωση του μεγέθους του νεοπλάσματος. Υπάρχουν διάφορα πρωτόκολλα ακτινοθεραπείας και αφορούν είτε στην κλασματική (fractionated) είτε στην υποκλασματική (hypofractionated) ακτινοθεραπεία.8,50 Μια από τις μεγαλύτερες έρευνες που έχουν πραγματοποιηθεί, αφορούσε 25 σκύλους με έντονα διηθητικό καρκίνωμα του θυρεοειδή αδένα που δεν παρουσίαζαν μεταστάσεις και υποβλήθηκαν σε υποκλασματική ακτινοθεραπεία. Τα ποσοστά επιβίωσης -ανεξαρτήτως της εξέλιξης του νεοπλάσματος- ανέρχονταν στο 80% 1 χρόνο μετά και στο 72% 3 χρόνια μετά. Ο χρόνος στον οποίο τα νεοπλάσματα έφτασαν στο μικρότερο μέγεθός τους κυμαίνονταν μεταξύ 8-22 μηνών, ενώ μόνο το 28% των ζώων εμφάνισε μετάσταση σε άλλες περιοχές.8 Σε μία άλλη μικρότερη έρευνα που έγινε σε σκύλους με διηθητικό καρκίνωμα του θυρεοειδή, οι οποίοι υποβλήθηκαν σε κλασματική ακτινοθεραπεία, ο μέσος χρόνος επιβίωσης ήταν τα 2 έτη.49 Τόσο τα υποκλασματικά όσο και τα κλασματικά πρωτόκολλα δίνουν πολύ καλά αποτελέσματα σε ότι αφορά τον χρόνο επιβίωσης και την εμφάνιση μεταστάσεων.8,50
Θεραπεία με ραδιενεργό Ιώδιο (131I)
Η θεραπεία με 131I προτείνεται στις περιπτώσεις διηθητικών καρκινωμάτων ή παρουσίας μεταστατικών εστιών και γίνεται συνδυαστικά ή όχι με τη χειρουργική θεραπεία. Από σχετικές έρευνες που έχουν πραγματοποιηθεί φαίνεται πως μπορεί να παρατείνει σημαντικά τον χρόνο επιβίωσης των ζώων.9,13 Σε μια μεγάλη μελέτη σε 65 σκύλους με καρκίνωμα του θυρεοειδή, στους 43 από αυτούς πραγματοποιήθηκε θεραπεία με131I (1-3 συνεδρίες131I σε δόση 555- 1850 MBq) σε συνδυασμό με ή χωρίς χειρουργική θεραπεία, ενώ, στους υπόλοιπους δεν πραγματοποιήθηκε καμία θεραπεία. Ο μέσος χρόνος επιβίωσης ήταν οι 34, 30, και 3 μήνες, αντίστοιχα.9
Χημειοθεραπεία
Η χημειοθεραπεία χρησιμοποιείται σε ζώα με διηθητικά καρκινώματα ή/και παρουσία μεταστατικών εστιών σε συνδυασμό ή όχι με τη χειρουργική επέμβαση. Η αποτελεσματικότητα της όμως, προς το παρόν, αμφισβητείται. Σε μια μελέτη στην οποία χορηγούνταν δοξορουβικίνη ως αποκλειστική θεραπεία, στο 40% των ασθενών το καρκίνωμα είχε μειωθεί περισσότερο από το μισό και είχαν μέσο χρόνο επιβίωσης της 37 εβδομάδες.51 Σε μια άλλη μελέτη στην οποία χορηγούταν σισπλατίνη, το 54% των ζώων παρουσίασε μείωση του μεγέθους του νεοπλάσματος μεγαλύτερη από το 50% και είχε μέσο χρόνο επιβίωσης 322 ημέρες. Όμως στα περισσότερα από τα ζώα αυτά είχε χορηγηθεί προηγουμένως δοξορουβικίνη, γεγονός που καθιστά δύσκολη την εκτίμηση του αποτελέσματος. Το υπόλοιπο 46% των ζώων παρουσίασε μέσο χρόνο επιβίωσης 98 ημέρες.14 Σε μια πρόσφατη μελέτη σε 44 ζώα πραγματοποιήθηκε χημειοθεραπεία με διάφορα χημειοθεραπευτικά (καρβοπλατίνη, σισπλατίνη, δοξορουβικίνη ή γεμσιταβίνη) ως μονοθεραπεία ή σε συνδυασμό με χειρουργική θεραπεία. Οι μέσοι χρόνοι επιβίωσης των ζώων δεν διέφεραν σημαντικά ανάμεσα στις δύο ομάδες.52
> Βιβλιογραφία
1. Brodey RS, Kelly DF. Thyroid neoplasms in the dog. A clinicopathologic study of fifty-seven cases. Cancer 1968, 22: 406-416.
2. Birchard SJ, Roesel OF. Neoplasia of the thyroid gland in the dog: a retrospective study of 16 cases. J Am Anim Hosp Assoc 1981, 17: 369-372.
3. Hararι J, Patterson JS, Rosenthal RC. Clinical and pathologic features of thyroid tumors in 26 dogs. J Am Vet Med Assoc 1986, 188: 1160-1164.
4. Wucherer KL, Wilke V. Thyroid Cancer in Dogs: An Update Based on 638 Cases (1995-2005). J Am Anim Hosp Assoc 2010, 46: 249-254.
5. Loar AS. Canine thyroid tumors. In Current Veterinary Therapy IX. Kirk RW (ed). WB Saunders: Philadelphia, 1986, pp. 1033-1039.
6. Barber LG. Thyroid tumors in dogs and cats. Vet Clin North Am Small Anim Pract 2007, 37: 755-773.
7. Klein MK, Powers BE, Withrow SJ, Curtis CR, Straw RC, Ogilvie GK, Dickinson KL, Cooper MF, Baier M. Treatment of thyroid carcinoma in dogs by surgical resection alone: 20 cases (1981-1989). J Am Vet Med Assoc 1995, 206: 1007-1009.
8. Théon AP, Marks SL, Feldman ES, Griffey S. Prognostic factors and patterns of treatment failure in dogs with unresectable differentiated thyroid carcinomas treated with megavoltage irradiation. J Am Vet Med Assoc 2000, 216: 1775-1779.
9. Worth AJ, Zuber RM, Hocking M. Radioiodide (131) I therapy for the treatment of canine thyroid carcinoma. Aust Vet J 2005, 83: 208-14.
10. Carver JR, Kapatkin A, Patnaik AK. A Comparison of medullary thyroid carcinoma and thyroid adenocarcinoma in dogs: A retrospective study of 38 cases. Vet Surg 1995, 24: 315-319.
11. Leav I, Schiller AL, Rijnberk A, Legg MA, Der Kinderen PJ. Adenomas and Carcinomas of the Canine and Feline Thyroid. Am J Pathol 1976, 83: 61-122.
12. Hayes HM, Fraumeni JF. Canine thyroid neoplasms: epidemiologic features. J Natl Cancer Inst 1975, 55: 931-934.
13. Turrel JM, McEntee MC, Bruke BP, Page RL. Sodium iodide I 131 treatment of dogs with nonresectable thyroid tumors: 39 cases (1990-2003). J Am Vet Med Assoc 2006, 229: 542-548.
14. Fineman LS, Hamilton TA, Gortari A, Bonney P. Cisplatin chemotherapy for treatment of thyroid carcinoma in dogs: 13 cases. J Am Anim Hosp Assoc 1998, 34: 109-112.
15. Benjamin SA, Saunders WJ, Angleton GM, Lee AC. Radiation carcinogenesis in dogs irradiated during prenatal and postnatal development. J Radiat Res 1991, 32: 86-103.
16. Verschueren CP, Rutteman GR, Vos JH, Van Dijk JE, De Bruin TW. Thyrotrophin receptors in normal and neoplastic (primary and metastatic) canine thyroid tissue. J Endocrinol 1992, 132: 461-468.
17. Benjamin SA, Stephens LC, Hamilton BF, Saunders WJ, Lee AC, Angleton GM, Mallinckrodt CH. Associations between lymphocytic thyroiditis, hypothyroidism, and thyroid neoplasia in beagles. Vet Pathol 1996, 33: 486-494.
18. Suarez HG, du Villard JA, Severino M, Caillou B, Schlumberger M, Tubiana M et al. Presence of mutations in all three ras genes in human thyroid tumors. Oncogene 1990, 5: 565-570.
19. Kondo T, Ezzat S, Asa SL. Pathogenetic mechanisms in thyroid follicular-cell neoplasia. Nat Rev Cancer 2006, 6: 292-306.
20. Verschueren CP. Flow-Cytometric DNA Ploidy analysis in primary and metastatic canine thyroid carcinomas. Anticancer Res 1991, 11: 1755-1761.
21. Bertazzolo W, Giudice C, Dell’Orco M, Caniatti M. Paratracheal cervical mass in a dog. Vet Clin Pathol 2003, 32: 209-212.
22. Almes KM, Heaney AM, Andrews JA. Intracardiac ectopic thyroid carcinosarcoma in a dog. Vet Pathol 2008, 45: 500-504.
23. Lantz GC, Salisbury SK. Surgical excision of ectopic thyroid carcinoma involving the base of the tongue in dogs: three cases (1980-1987). J Am Vet Med Assoc 1989, 195: 1606-1608.
24. Broome MR, Peterson ME, Walker JR. Clinical features and treatment outcomes of 41 dogs with sublingual ectopic thyroid neoplasia. J Vet Intern Med 2014, 28: 1560-1568.
25. Liptak JM, Kamstock DA, Dernell WS, Ehrhart EJ, Rizzo SA, Withrow SJ. Cranial mediastinal carcinomas in nine dogs. Vet Comp Oncol 2008, 6: 19-30.
26. Constantino-Casas F, Rodriguez-Martinez HA, Gutierrez Diaz- Ceballos ME. A case report and review: the gross, histological and immunohistochemical characteristics of a carcinoma of ectopic thyroid in a dog. Br Vet J 1996, 152: 669-672.
27. Kiupel M, Capen C, Miller M, Smedley R. Histological classification of the endocrine system of domestic animals Washington. Armed Forces Institute of Pathology, 2008, pp. 64-68.
28. Patnaik AK, Lieberman PH. Gross, histologic, cytochemical and immunocytochemical study of medullary carcinoma in sixteen dogs. Vet Pathol 1991, 28: 223-233.
29. Susaneck SJ. Thyroid tumors in the dog. Compend Cont Educ Pract Vet 1983, 5: 35-38.
30. Taeymans O, Peremans K, Saunders JH. Thyroid imaging in the dog: current status and future directions. J Vet Intern Med 2007, 21: 673-684.
31. Simpson AC, McCown JL. Systemic hypertension in a dog with a functional thyroid gland adenocarcinoma. J Am Vet Med Assoc 2009, 235:1474-1479.
32. Seguin B, Brownlee L, Walsh PJ. Endocrine system. In Veterinary Surgical Oncology. Kudnig ST, Sequin B(eds). Wiley-Blackwell: Chichester, 2012, pp. 405- 441.
33. Wisner ER, Nyland TG. Ultrasonography of the thyroid and parathyroid glands. Vet Clin North Am Small Anim Pract 1998, 28: 973-991.
34. Weber AL, Randolph G, Aksoy FG. The thyroid and parathyroid glands. CT and MR imaging and correlation with pathology and clinical findings. Radiol Clin North Am 2000, 38: 1105-1129.
35. Feldman N. Canine thyroid tumors and hyperthyroidism. In Canine and Feline Endocrinology and Reproduction. Feldman N (ed). 3rd ed. Saunders: Philadelphia, 2003, pp. 219-249.
36. Taeymans O, Penninck DG, Peters RM. Comparison between clinical, ultrasound, CT, MRI, and pathology findings in dogs presented for suspected thyroid carcinoma. Vet Radiol Ultrasound 2013, 54: 61-70.
37. Taeymans O, Schwarz T, Duchateau L, Barberet V, Gielen I, Haskins M, van Bree H, Saunders J. Computed tomographic features of the normal canine thyroid gland. Vet Radiol Ultrasound 2008, 49: 13-19.
38. Liptak JM. Canine thyroid carcinoma. Clin Tech Small Anim Pract 2007, 22: 75-78.
39. Flanders JA. Surgical therapy of the thyroid. Vet Clin North Am Small Anim Pract 1994 , 24: 607-621.
40. Kent MS, Griffey SM, Verstraete FJ, Naydan D, Madewell BR. Computerassisted image analysis of neovascularization in thyroid neoplasms from dogs. Am J Vet Res 2002, 63: 363-369.
41. Sullivan M, Cox F, Pead MJ, McNell P. Thyroid tumours in the dog. J Small Anim Pract 1987, 28: 505-512.
42. Owen LN. TNM Classification of Tumours in Domestic Animals. 1st ed. World Health Organization: Geneva, 1980, pp. 51-53.
43. Lunn KF, Page RL. Tumors of the endocrine system. In Withrow and Mac- Ewen’s Small Animal Clinical Oncology. Withrow SJ, Vail DM, Page RL (eds) 5th ed. Elsevier: St Louis, 2013, pp. 504-531.
44. Michail S. Comparative Anatomy of the Domestic Animals. 2nd edn. D Kyriakidis: Thessaloniki, 2015.
45. Hullinger RL. The endocrine system. In Miller’s Anatomy of the Dog. Evans HE (ed). 3rd ed. WB Saunders Co: Philadelphia, 1993, pp. 559-585.
46. Radlinsky MG. Thyroid surgery in dogs and cats. Vet Clin Small Anim 2007, 37: 789-798.
47. Fukui S, Endo Y, Hirayama K, Taniyama H, Kadosawa T. Identification and preservation of the parathyroid gland during total thyroidectomy in dogs with bilateral thyroid carcinma: a report of six cases. J Vet Med Sci 2015, 77: 747-751.
48. Kornegay JN. Hypocalcemia in dogs. Compend Cont Educ Pract Vet 1982, 4: 103-110.
49. Tuohy JL, Worley DR Withrow SJ. Outcome following simultaneous bilateral thyroid lobectomy for treatment of thyroid gland carcinoma in dogs: 15 cases (1994–2010). J Am Vet Med Assoc 2012, 241: 95-103.
50. Pack L, Roberts R, Dawson SD, Dookwah HD. Definitive radiation therapy for infiltrative thyroid carcinoma in dogs. Vet Radiol Ultrasound 2001, 42: 471-474.
51. Jeglum KA, Whereat A. Chemotherapy of canine thyroid carcinoma. Compend Cont Educ Pract Vet 1983, 5: 96-98.
52. Nadeau ME, Kitchell BE. Evaluation of the use of chemotherapy and other prognostic variables for surgically excised canine thyroid carcinoma with and without metastasis. Can Vet J 2011, 52: 994-998.












 PDF Download
PDF Download Η αφορμή για αυτό το άρθρο σύνταξης ήταν η δημοσίευση από την Παγκόσμια Εταιρεία Ιατρικής Ζώων Συντροφιάς (WSAVA) κατευθυντήριων οδηγιών για την κτηνιατρική οδοντιατρική, ενός σημαντικού πονήματος 165 σελίδων. Η ΕΛΕΚΖΣ ανέλαβε τη μετάφραση των οδηγιών στην ελληνική γλώσσα, με στόχο να τις διανείμει στα μέλη της στο 10ο επετειακό Forum το Μάρτιο του 2019. Ιστορικά, η οδοντιατρική στην κτηνιατρική επιστήμη φαίνεται πως εφαρμόστηκε αιώνες π.Χ. στα ιπποειδή, μάλιστα υπάρχουν σχετικές αναφορές για αντιμετώπιση προβλημάτων των δοντιών και αναγνώριση της ηλικίας ιπποειδών ήδη από το 6ο αιώνα π.Χ. στην Κίνα. Στην αρχαία Ελλάδα φαίνεται πως βελτιώθηκε η τεχνική της αναγνώρισης της ηλικίας των ιπποειδών μέσω της οδοντοφυίας τους. Ο Σίμων ο Αθηναίος, τον 5ο αιώνα π.Χ., στο βιβλίο του «Κτηνιατρική τέχνη, η εκτιμητική των ιπποειδών», αναφέρεται στις ηλικίες ανατολής των δοντιών των ίππων και στον τρόπο εκτίμησης της ηλικίας τους. Μεταγενέστερα, το 333 π.Χ., ο Αριστοτέλης στο βιβλίο του «Ιστορία των ζώων» δίνει έναν ορισμό της περιοδοντικής νόσου των ίππων, ενώ τη σκυτάλη πήραν οι Ρωμαίοι, οι οποίοι και ανέπτυξαν σημαντικά την οδοντιατρική των ιπποειδών. Στη σύγχρονη εποχή πρωτεργάτης στην οδοντιατρική ζώων συντροφιάς (ΟΖΣ) ήταν ο Joseph Bodingbauer τη δεκαετία του 1930 στη Βιέννη, ενώ στις Η.Π.Α. το πεδίο αυτό της κτηνιατρικής επιστήμης ξεκίνησε να αναπτύσσεται σχετικά πρόσφατα και κυρίως μετά το 1970. Συγκεκριμένα αναγνωρίστηκε ως ξεχωριστή ειδικότητα της κτηνιατρικής επιστήμης το 1988 στις Η.Π.Α., με την ίδρυση του Αμερικανικού Κολλεγίου Κτηνιατρικής Οδοντιατρικής (AVDC) και στην Ευρώπη τo 1998 με την ίδρυση του Ευρωπαϊκού Κολλεγίου Κτηνιατρικής Οδοντιατρικής (EVDC). Η πρώτη κτηνιατρική σχολή που δημιούργησε τμήμα κτηνιατρικής οδοντιατρικής ήταν η Κτηνιατρική Σχολή του Πανεπιστημίου της Πενσυλβάνια (U-Penn) στη Φιλαδέλφεια των Η.Π.Α. στη δεκαετία του 1970, με πρωτοπόρο τον καθηγητή χειρουργικής Colin Harvey, o οποίος πρόσφατα τιμήθηκε από τη WSAVA στο Παγκόσμιο Συνέδριο Κτηνιατρικής Μικρών Ζώων στη Σιγκαπούρη για τη μεγάλη του συμβολή στην ανάπτυξη της κτηνιατρικής οδοντιατρικής. Η ανάπτυξη της ΟΖΣ είναι ραγδαία τις τελευταίες δύο δεκαετίες και σύμφωνα με πολλούς συγγραφείς οι οδοντιατρικές, οι στοματολογικές και οι γναθοπροσωπικές παθήσεις αποτελούν τις συχνότερες παθήσεις που αντιμετωπίζονται στην κτηνιατρική των ζώων συντροφιάς, ενώ στη Βόρεια Αμερική και στην Ευρώπη σημαντικό μέρος των εσόδων ενός κτηνιατρείου προκύπτει από την ΟΖΣ.
Η αφορμή για αυτό το άρθρο σύνταξης ήταν η δημοσίευση από την Παγκόσμια Εταιρεία Ιατρικής Ζώων Συντροφιάς (WSAVA) κατευθυντήριων οδηγιών για την κτηνιατρική οδοντιατρική, ενός σημαντικού πονήματος 165 σελίδων. Η ΕΛΕΚΖΣ ανέλαβε τη μετάφραση των οδηγιών στην ελληνική γλώσσα, με στόχο να τις διανείμει στα μέλη της στο 10ο επετειακό Forum το Μάρτιο του 2019. Ιστορικά, η οδοντιατρική στην κτηνιατρική επιστήμη φαίνεται πως εφαρμόστηκε αιώνες π.Χ. στα ιπποειδή, μάλιστα υπάρχουν σχετικές αναφορές για αντιμετώπιση προβλημάτων των δοντιών και αναγνώριση της ηλικίας ιπποειδών ήδη από το 6ο αιώνα π.Χ. στην Κίνα. Στην αρχαία Ελλάδα φαίνεται πως βελτιώθηκε η τεχνική της αναγνώρισης της ηλικίας των ιπποειδών μέσω της οδοντοφυίας τους. Ο Σίμων ο Αθηναίος, τον 5ο αιώνα π.Χ., στο βιβλίο του «Κτηνιατρική τέχνη, η εκτιμητική των ιπποειδών», αναφέρεται στις ηλικίες ανατολής των δοντιών των ίππων και στον τρόπο εκτίμησης της ηλικίας τους. Μεταγενέστερα, το 333 π.Χ., ο Αριστοτέλης στο βιβλίο του «Ιστορία των ζώων» δίνει έναν ορισμό της περιοδοντικής νόσου των ίππων, ενώ τη σκυτάλη πήραν οι Ρωμαίοι, οι οποίοι και ανέπτυξαν σημαντικά την οδοντιατρική των ιπποειδών. Στη σύγχρονη εποχή πρωτεργάτης στην οδοντιατρική ζώων συντροφιάς (ΟΖΣ) ήταν ο Joseph Bodingbauer τη δεκαετία του 1930 στη Βιέννη, ενώ στις Η.Π.Α. το πεδίο αυτό της κτηνιατρικής επιστήμης ξεκίνησε να αναπτύσσεται σχετικά πρόσφατα και κυρίως μετά το 1970. Συγκεκριμένα αναγνωρίστηκε ως ξεχωριστή ειδικότητα της κτηνιατρικής επιστήμης το 1988 στις Η.Π.Α., με την ίδρυση του Αμερικανικού Κολλεγίου Κτηνιατρικής Οδοντιατρικής (AVDC) και στην Ευρώπη τo 1998 με την ίδρυση του Ευρωπαϊκού Κολλεγίου Κτηνιατρικής Οδοντιατρικής (EVDC). Η πρώτη κτηνιατρική σχολή που δημιούργησε τμήμα κτηνιατρικής οδοντιατρικής ήταν η Κτηνιατρική Σχολή του Πανεπιστημίου της Πενσυλβάνια (U-Penn) στη Φιλαδέλφεια των Η.Π.Α. στη δεκαετία του 1970, με πρωτοπόρο τον καθηγητή χειρουργικής Colin Harvey, o οποίος πρόσφατα τιμήθηκε από τη WSAVA στο Παγκόσμιο Συνέδριο Κτηνιατρικής Μικρών Ζώων στη Σιγκαπούρη για τη μεγάλη του συμβολή στην ανάπτυξη της κτηνιατρικής οδοντιατρικής. Η ανάπτυξη της ΟΖΣ είναι ραγδαία τις τελευταίες δύο δεκαετίες και σύμφωνα με πολλούς συγγραφείς οι οδοντιατρικές, οι στοματολογικές και οι γναθοπροσωπικές παθήσεις αποτελούν τις συχνότερες παθήσεις που αντιμετωπίζονται στην κτηνιατρική των ζώων συντροφιάς, ενώ στη Βόρεια Αμερική και στην Ευρώπη σημαντικό μέρος των εσόδων ενός κτηνιατρείου προκύπτει από την ΟΖΣ.
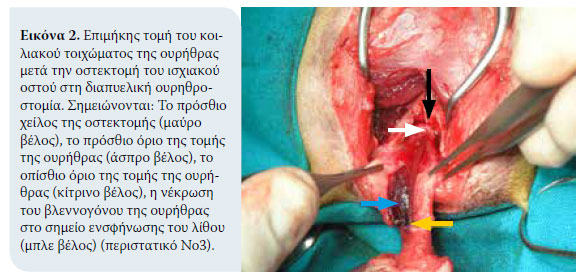
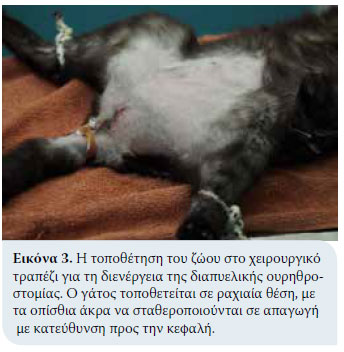 1. Τοποθέτηση του γάτου και αντισηψία
1. Τοποθέτηση του γάτου και αντισηψία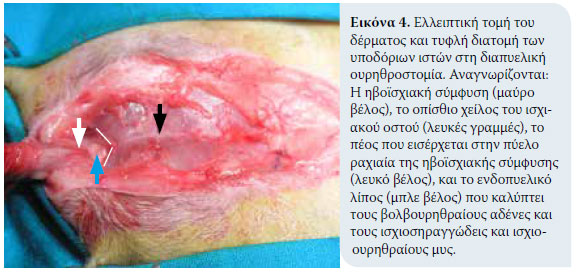




 Στα περιστατικά αδενώματος του θυρεοειδή, η χειρουργική εξαίρεση του νεοπλάσματος αποτελεί την θεραπεία εκλογής και οδηγεί στην ίαση του ζώου.6,32 Αναφορικά με το καρκίνωμα του θυρεοειδή η επιλογή θεραπείας εξαρτάται από παράγοντες όπως το μέγεθος του όγκου, το βαθμό διήθησης των γειτονικών ιστών, την παρουσία μεταστάσεων και τη δυνατότητα χρησιμοποίησης άλλων θεραπευτικών μέσων (ακτινοθεραπεία, χημειοθεραπεία).43 Γενικά, η χειρουργική θεραπεία ενδείκνυται στα περιστατικά μικρών (<7cm) και κινητών νεοπλασμάτων ή σε νεοπλάσματα με επιφανειακή διήθηση των γειτονικών ιστών, ενώ, αντενδείκνυται στις περιπτώσεις έντονα διηθητικών και μη κινητών νεοπλασμάτων (Εικόνα6).6,7,10,32 Πολλές φορές είναι απαραίτητη η χειρουργική διερεύνηση του καρκινώματος για να διαπιστωθεί ο βαθμός διήθησης των γειτονικών ιστών. Στα περιστατικά που διαγιγνώσκονται με μεταστατική νόσο, η θεραπεία που αναλαμβάνεται είναι παρηγορητική και περιλαμβάνει την ακτινοθεραπεία ή τη χορήγηση ραδιενεργού ιωδίου ή το συνδυασμό χειρουργική εξαίρεσης και ακτινοθεραπείας. Όταν μετά τον απεικονιστικό έλεγχο δεν διαπιστωθούν μεταστάσεις, η επιλογή της θεραπείας θα βασιστεί στο κατά πόσο το νεόπλασμα είναι κινητό ή όχι. Εφόσον είναι κινητό, επιλέγεται η χειρουργική εξαίρεση του, πραγματοποιώντας ετερόπλευρη ή σπάνια αμφοτερόπλευρη θυρεοειδεκτομή, συνδυαστικά ή όχι με ακτινοθεραπεία. Εφόσον το νεόπλασμα είναι μη κινητό, η χειρουργική θεραπεία αντενδείκνυται και προτείνονται ακτινοθεραπεία και θεραπεία με ραδιενεργό ιώδιο.32
Στα περιστατικά αδενώματος του θυρεοειδή, η χειρουργική εξαίρεση του νεοπλάσματος αποτελεί την θεραπεία εκλογής και οδηγεί στην ίαση του ζώου.6,32 Αναφορικά με το καρκίνωμα του θυρεοειδή η επιλογή θεραπείας εξαρτάται από παράγοντες όπως το μέγεθος του όγκου, το βαθμό διήθησης των γειτονικών ιστών, την παρουσία μεταστάσεων και τη δυνατότητα χρησιμοποίησης άλλων θεραπευτικών μέσων (ακτινοθεραπεία, χημειοθεραπεία).43 Γενικά, η χειρουργική θεραπεία ενδείκνυται στα περιστατικά μικρών (<7cm) και κινητών νεοπλασμάτων ή σε νεοπλάσματα με επιφανειακή διήθηση των γειτονικών ιστών, ενώ, αντενδείκνυται στις περιπτώσεις έντονα διηθητικών και μη κινητών νεοπλασμάτων (Εικόνα6).6,7,10,32 Πολλές φορές είναι απαραίτητη η χειρουργική διερεύνηση του καρκινώματος για να διαπιστωθεί ο βαθμός διήθησης των γειτονικών ιστών. Στα περιστατικά που διαγιγνώσκονται με μεταστατική νόσο, η θεραπεία που αναλαμβάνεται είναι παρηγορητική και περιλαμβάνει την ακτινοθεραπεία ή τη χορήγηση ραδιενεργού ιωδίου ή το συνδυασμό χειρουργική εξαίρεσης και ακτινοθεραπείας. Όταν μετά τον απεικονιστικό έλεγχο δεν διαπιστωθούν μεταστάσεις, η επιλογή της θεραπείας θα βασιστεί στο κατά πόσο το νεόπλασμα είναι κινητό ή όχι. Εφόσον είναι κινητό, επιλέγεται η χειρουργική εξαίρεση του, πραγματοποιώντας ετερόπλευρη ή σπάνια αμφοτερόπλευρη θυρεοειδεκτομή, συνδυαστικά ή όχι με ακτινοθεραπεία. Εφόσον το νεόπλασμα είναι μη κινητό, η χειρουργική θεραπεία αντενδείκνυται και προτείνονται ακτινοθεραπεία και θεραπεία με ραδιενεργό ιώδιο.32




 > Κλινικό Περιστατικό
> Κλινικό Περιστατικό